- 相關法規 -
19.May.2014
拉曼-Roman PIC/S GMP急上路,必"藥"把關
為確保製藥品質及民眾用藥安全,臺灣自1982年開始要求藥品製造須符合藥品優良製造規範(Good Manufacturing Practice,GMP),並不斷隨著品質觀念的革新及國際GMP標準的提升與調和一致化,逐步更新國內西藥GMP的規範,於2010年起正式採用國際通用之PIC/S GMP標準,並訂於2014年12 月31日前,所有西藥製劑廠將全面完成實施。

PIC/S GMP簡介與影響PIC/S GMP中文全名:「國際醫藥品稽查協約組織」,為外觀橘紅色6角型標章,內有臺灣地圖,且印上PIC/S GMP等字樣,底下則有Taiwan FDA;食藥局局長-康照洲說,有了這個標章,代表製藥品質比GMP更好,因為PIC/S GMP是目前全球公認最嚴謹的製藥規範。
2015年1月1日起,所有國產藥物都必須貼上PIC/S GMP標章,才能夠上市販售。
PIC/S GMP相關條文
PIC/S GMP1.3提到「正確的原物料、容器和標籤」是做好GMP的條件之一。如何確認原物料、容器跟標籤的品質,除了做好供應商管理、訂定完善的接收程式外,透過檢驗更能進一步確認其是否符合既定的規格。
而PIC/S GMP 5.28提到,原物料之一次的交貨是由不同的批次所組成者,則為其抽樣、測試與放行,每一批次應各自考慮。不同的生產批次,應該每一個批次都要分別抽樣、測試跟放行,不能混為一批來看。
PIC/S GMP 5.30 是大家很關注的原料開封抽樣鑒別的規定。在條文內容提到:「應有適當的程式或措施來確保每個原料容器之內容物的同一性」。
關於100%開封抽樣鑒別,在PIC/S GMP附則8-2也有相關規定,「原料之完整批次的鑒識、通常只有在自全部容器中抽取個別樣品,並對每一樣品執行鑒別試驗時始能確保」。對於如何「建立確效程式來確保無任何原料容器會被不正確的標識者,可容許只對一定比例之容器抽樣」。
如何檢測藥品之原物料
根據PIC/S GMP法規,我們必需對藥品之原物料進行檢驗,以確保標籤、批次、同一性、抽樣,整理如下表:
| 條文 | 內容綱要 |
| PIC/S GMP1.3 | 確認原物料、容器跟標籤的品質,除了做好供應商管理、訂定完善的接收程式外,透過檢驗能確認是否符合規格 |
| PIC/S GMP 5.28 | 確保不同批次都要分別抽樣、測試跟放行 |
| PIC/S GMP 5.30 | 確保同一批,每個原料容器之內容物的同一性 |
| PIC/S GMP 附則8-2 |
原料之完整批次的鑒識、通常只有在自全部容器中抽取個別樣品,並對每一樣品執行鑒別試驗時始能確保 |

面對藥廠如此大量的原物料檢驗,如果採用「高效液相層析法(HPLC)、層析(GC、LC…等)」來檢測,通常需要花費超過1小時,除了時間及成本較高外,恐實行上會面臨許多困難。
如果選擇「掌上型-紅外線光譜儀(FTIR、NIR…等)」,雖然速度上有比較好的表現,但因為解析度關係,較常產生很大的誤差,且無法測試含水的樣品,造成很大的困擾。
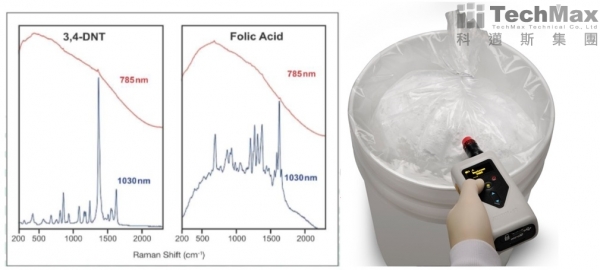
因此,使用「掌上型-拉曼光譜儀」進行快篩,不僅有較好的光譜解析度,且輕便、快速、無需樣品製作準備、即便隔著塑膠包、玻璃瓶,皆能立即檢測出可靠結果,如右圖,可在短時間內,立即顯示原物料之PASS/FAIL。
結論
藥品的把關日趨嚴格, 由其2015年1月1日PIC/S GMP標章即將上路,唯有通過規範,才能在市場上販售,透過「掌上型拉曼光譜儀」不僅能對原物料進行檢驗、確定標籤無誤、各批次檢測確保、同批次同一性確認、抽樣檢查…等應用,最重要的是儀器的輕便、快速、無需樣品製作準備、隔著塑膠包、玻璃瓶,皆能立即檢測出可靠資料…等優勢,才是現場大量快篩,真正實用的唯一選擇。

其他相關訊息
-
04.Mar.2024
X-ray螢光-XRF 原能會改制? 別擔心,科邁斯一站式服務讓您無後顧之憂!
-
26.Feb.2024
X-ray螢光-XRF 面對RoHS 3.0新添限制物質該如何對應?
-
02.Jan.2024
X-ray螢光-XRF 何種XRF貴金屬分析儀適合您?









